Molecure poinformowało wczoraj po południu, że nie dostało pozwolenia na przeprowadzenie badania klinicznego fazy II dla cząsteczki OATD-01 u pacjentów z aktywną sarkoidozą płucną na terytorium Unii Europejskiej oraz Norwegii.
Zarząd spółki przekazała, że niezwłocznie złoży nowy wniosek, wprowadzając przy tym odpowiednie zmiany, które pozwolą Molecure otrzymać zgody wszystkich urzędów regulacyjnych w wybranych przez spółkę państwach członkowskich.
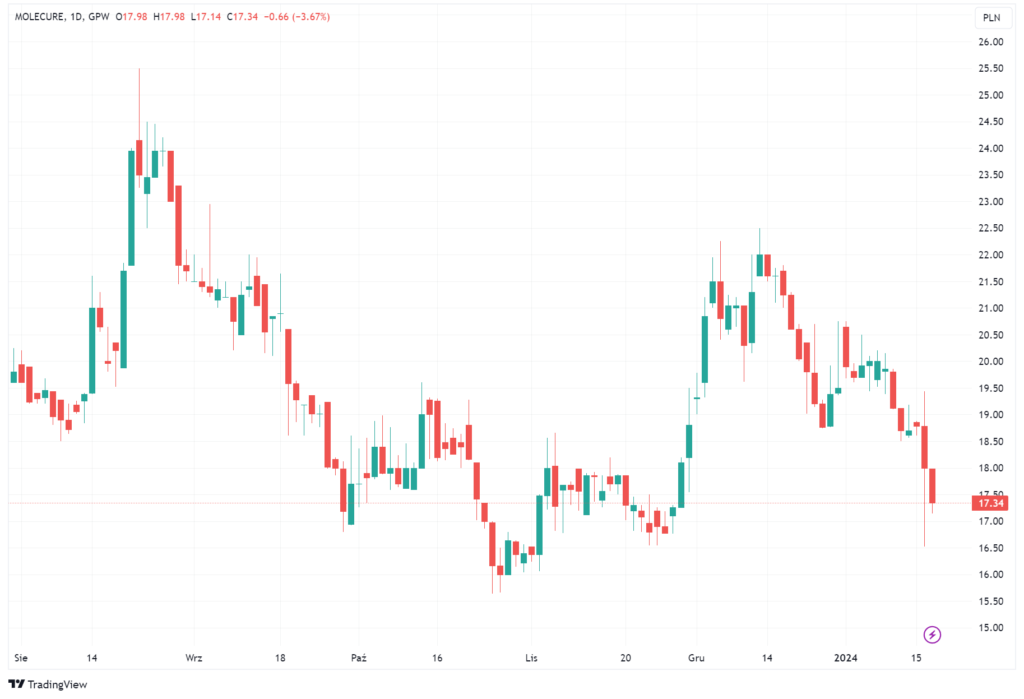
Informacja o otrzymaniu odmowy wydania pozwolenia na przeprowadzenie badania przez Molecure poważnie zaniepokoiła inwestorów. W efekcie, na rynku od wczoraj rządzi podaż. We wtorek akcje Molecure potaniały o 4,2%, a dziś wyprzedaż jest kontynuowana. W tej chwili walory spółki tracą 3,7%.
Molecure nie może przeprowadzić II fazy badania klinicznego w UE i Norwegii 
W oficjalnym komunikacie Molecure przekazało, że “jedną z przyczyn odmowy wydania pozwolenia na prowadzenie badania klinicznego był, w odniesieniu do Polski, dodatkowy rygorystyczny warunek dotyczący ograniczenia stopnia ekspozycji pacjentów biorących udział w badaniu klinicznym na promieniowanie w toku procedur medycznych wykonywanych w trakcie badania klinicznego, w szczególności badania obrazowego metodą PET/CT (co stanowi metodę diagnostyczną dla zakładanego punktu końcowego oceny skuteczności badanego leku)”.
We wczorajszym komunikacie możemy przeczytać też, że “pozostałe szczegółowe przyczyny odmowy wydania zgody na prowadzenie badania klinicznego są obecnie analizowane przez emitenta”.
Molecure poinformowało przy tym, że “pomimo otrzymania przez spółkę cząstkowych zgód wszystkich właściwych komisji etycznych, odmowną decyzję wydał polski Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych oraz Produktów Biobójczych”.
Spółka wyjaśniła bowiem, iż “jako że Polska pełniła w procesie skoordynowanego rozpoznawania wniosku spółki rolę państwa sprawozdawcy, z uwagi na przepisy prawa regulujące procedurę uzyskiwania zgody na prowadzenie badań klinicznych w Unii Europejskiej, odmowna decyzja państwa pełniącego rolę sprawozdawcy skutkuje niemożliwością prowadzenia badania klinicznego we wszystkich państwach, których wniosek dotyczył, niezależnie od indywidualnych stanowisk tych państw zajętych w toku procedury”.
Partnerem portalu Portfel Polaka jest Plantwear S.A., polski producent zegarków i biżuterii, oferujący najwyższej jakości produkty wykonane z naturalnych surowców: drewna i kamieni szlachetnych. Odkryj piękno i unikalność modowych dodatków.
W oficjalnym komunikacie napisano ponadto, że “spółka analizuje scenariusze, które pozwolą jej na możliwie najszybsze ponowne złożenie wniosku o wydanie pozwolenia na przeprowadzenie badania klinicznego fazy II dla cząsteczki OATD-01 u pacjentów z aktywną sarkoidozą płucną, wprowadzając przy tym niezbędne zmiany, które pozwolą spółce otrzymać zgody wszystkich urzędów regulacyjnych w wybranych przez spółkę państwach członkowskich”.
Molecure zgodnie z planem rozpocznie badania kliniczne w USA i Wielkiej Brytanii
Molecure jednocześnie przypomniało, że otrzymało już w wyżej wymienionym zakresie niezbędną zgodę amerykańskiej Agencji Żywności i Leków, a następnie amerykańskiego ciała będącego odpowiednikiem komisji etycznej, a także otrzymała zgodę brytyjskiej komisji etycznej oraz brytyjskiego Urzędu Rejestracji Produktów Leczniczych i Wyrobów Medycznych.
Molecure oznajmiło, że w związku z tym “spółka zgodnie z planem rozpocznie w najbliższym czasie prowadzenie wyżej wymienione badania klinicznego, mającego na celu określenie skuteczności klinicznej, farmakokinetyki, farmakodynamiki oraz bezpieczeństwa OATD-01 u pacjentów z aktywną sarkoidozą płucną na terytorium Wielkiej Brytanii oraz Stanów Zjednoczonych. W USA proces przygotowania badania klinicznego przebiega bez zakłóceń i spółka finalizuje etap kontraktowania ostatnich ośrodków”. 
Warto wyjaśnić, że opisywane badanie jest docelowo podwójnie zaślepionym, z kontrolą placebo, wieloośrodkowym (25-30 ośrodków w Europie i Stanach Zjednoczonych) badaniem klinicznym fazy II, ze stałą dawką podawanego przez 12 tygodni związku OATD-01.
Molecure przewiduje, że włączenie pierwszego pacjenta nastąpi w pierwszym kwartale 2024 roku, a samo badanie kliniczne będzie trwało od 19 do 25 miesięcy od pierwszego podania do raportu końcowego. W badaniu weźmie udział około 90 pacjentów.
Cząsteczka OATD-01 wykazała już potencjał modyfikowania przebiegu choroby w badaniach przedklinicznych. Molecure uważa, że OATD-01 może stać się nowym standardem medycznym w leczeniu sarkoidozy płuc.
Prezes Molecure o decyzji polskiego urzędu
Prezes Molecure, Marcin Szumowski oznajmił, że “jest zaskoczony i zawiedziony. Mimo że w toku oceny wniosku Molecure dokonało odpowiednich zmian w protokole badania i odniosło się do zastrzeżeń regulatora, otrzymało nieuzasadnione naukowo stanowisko polskiego urzędu regulacyjnego”.
Prezes Molecure stwierdził, że “Polska jest jedynym krajem w UE, w którym obowiązuje tak restrykcyjne podejście do diagnostyki radiologicznej w badaniach klinicznych, co potwierdzają radiolodzy z czołowych ośrodków klinicznych na świecie”.
Marcin Szumowski oświadczył przy tym, że „według wiedzy spółki odmowa nie była spowodowana kwestiami bezpieczeństwa badanej substancji. Molecure jest przygotowane na jak najszybsze ponowne złożenie wniosku na przeprowadzenie na terytorium Unii Europejskiej i Norwegii badania klinicznego drugiej fazy dla OATD-01 z wykluczeniem polskich ośrodków klinicznych i pacjentów ze względu na ograniczenia prawne dotyczące diagnostyki obrazowej”.
Akcje zniżkują
Wczorajszy komunikat o otrzymaniu odmowy wydania pozwolenia na przeprowadzenie badania klinicznego fazy II dla cząsteczki OATD-01 przez Molecure na terenie Unii Europejskiej i Norwegii poważnie zaniepokoiła uczestników rynku.
W efekcie, od wtorku mamy do czynienia z masową wyprzedażą akcji spółki. Wczoraj ich kurs spadł o 4,2%, a dziś papiery wartościowe Molecure tracą 3,7%.
O Molecure
Molecure, dawniej znane jako OncoArendi Therapeutics, to firma biotechnologiczna odkrywająca i rozwijająca leki do etapu klinicznego, wykorzystująca własne unikalne kompetencje w zakresie chemii medycznej oraz biologii do poszukiwania i opracowywania pierwszych w swojej klasie leków małocząsteczkowych, które poprzez bezpośrednią modulację niezbadanych dotąd celów białkowych i RNA mogą stanowić terapię wielu nieuleczalnych chorób.
Molecure wygenerowało zróżnicowane portfolio siedmiu odrębnych programów przy wsparciu wiodących akademickich instytucji naukowych na całym świecie, w tym Yale University, Rutgers University, Flemish Institute for Biotechnology (VIB) w Ghent, the University of Michigan oraz Międzynarodowego Instytutu Biologii Molekularnej i Komórkowej w Warszawie (MIBMiK).
Siedziba i laboratoria Molecure znajdują się w Warszawie oraz w Łodzi. Spółka jest notowana na Giełdzie Papierów Wartościowych w Warszawie od kwietnia 2018 roku.


